1. Die Krankheit
1.1 Der Erreger
Pneumokokken oder auch Streptococcus pneumoniae sind grampositive Bakterien die zur Gattung der Streptokokken gehören und sich als ei- bis lanzettförmige, bekapselte Diplokkokken zeigen.1 Die Gefährlichkeit des Erregers ist primär durch seine Kapsel, bestehend aus komplexen Kohlenhydraten, begründet. Diese spielt nicht nur eine Rolle in der lokalen Ansiedelung, sondern schützt auch vor dem Abbau durch Immunzellen und damit vor dem körpereigenen Immunsystem.2 Von der hoch-variablen Kapsel sind bisher >90 unterschiedliche Serotypen bekannt, die durch Verwandtschaft in 46 Serogruppen organisiert sind.2 Klinisch beeinflussen diese Gruppen Prognose, Therapie und Impfstrategie. Diagnostisch diese zu differenzieren ist und bleibt weiterhin jedoch eine Herausforderung.3
Im menschlichen Körper befinden sich Pneumokokken hauptsächlich im Nasenrachenraum. Durch lokale Verbreitung kann es zu Infektionen der oberen (Nasen-, Nasennebenhöhlen-, Mittelohrentzündung) und unteren (Lungenentzündung) Atemwege kommen.4 Bei Erwachsenen sind dabei die häufigsten Erkrankungen, die ambulant erworbenen Lungenentzündungen (community-acquired pneumonia, CAP) und die invasiven Pneumokokken-Erkrankungen (invasive pneumococcal disease, IPD).5 Die IPD werden durch den Nachweis von Pneumokokken in sonst sterilen Körperflüssigkeiten diagnostiziert, verlaufen schwerer und manifestieren sich primär in Form von einer Blutstrominfektion (Blut) und bakteriellen Hirnhautentzündung (Liquor). Seltener können sie im Rahmen einer Bauchfell-, Wurmfortsatz-, Herzinnenhautentzündung und bakteriellen Gelenkentzündungen nachgewiesen werden.4,6
1.2 Epidemiologie
Infektionen durch Pneumokokken können in jedem Lebensabschnitt eintreten, jedoch sind Kinder < 2 Jahren und Erwachsene > 65 Jahre Lebensalter besonders davon betroffen.7,8 Das Auftreten von durch Pneumokokken bedingten Erkrankungen variiert je nach Jahreszeit und häuft sich besonders zum Winter.9Übertragen wird der Erreger von Mensch zu Mensch durch Tröpfcheninfektionen.1 Daher begünstigen geringe Feuchtigkeit, enge Ansammlungen von Menschen in geschlossenen Räumen, virale Ko-Infektionen, kaltes Wetter und Luftverschmutzung, die Verbreitung des Erregers.10 In Deutschland sind Pneumokokken nur meldepflichtig bei direktem Nachweis des Erregers aus Nervenwasser, Blut, Gelenkflüssigkeit oder anderen, normalerweise sterilen Substraten.11,12 Aufgrund dessen ist es schwierig eine genaue Aussage über die Verbreitung des Erregers in der Bevölkerung zu treffen. Eine Studie aus England konnte jedoch zeigen, dass Kinder die größte Infektionsquelle darstellen (< 5Lj.: 48%; 5 – 20Lj.: 22%; > 20Lj.: 3%). Selbige Studie zeigte auch, dass durch den PCV13-Impfstoff (siehe Abschnitt 2), der Anteil der Serotypen, auf die der Impfstoff abzielt, von 75% auf ca. 5% reduziert werden konnte.13
Ambulant erworbene Pneumonien (CAP)
CAP sind weltweit auf Platz 3 der häufigsten Todesursachen und auf Platz 1 der häufigsten Todesursachen durch Infektionen.14
Besonders betroffen von ihnen sind ältere Menschen.5
Der häufigste identifizierte Erreger der CAP sind Pneumokokken, doch existiert in Deutschland kein System zur Überwachung des Auftretens von Pneumokokken-Pneumonien (PP).15
Europaweite Studien von erwachsenen Patienten zeigten, dass die generelle Inzidenz von CAP bei 68 – 7000/100.000 Einwohnern und die Anzahl an ins Krankenhaus eingewiesenen Fällen bei 16 – 3581/100.000 Einwohnern liegt.5
Das Robert-Koch-Institut (RKI) hat nach einer individualisierten Abfrage der Gesundheitsstatistik des Bundes (GBE) anhand der diagnostizierten Pneumonien und CAPNETZ-Studie, eines geschätzten Auftretens (20-60Lj.: 20/100.000; >60Lj.: 178/100.000; >65Lj.: 213/100.000) und Sterblichkeit (20-60Lj.: 1/100.000; >60Lj.: 24/100.000; >65Lj.: 30/100.000) über die PP herausgegeben.1
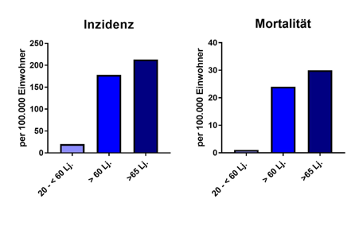
Abbildung 1: Geschätzte Inzidenz und Mortalität der Pneumokokken-Pneumonie nach individualisierter Abfrage des RKI bei der Gesundheitsstatistik des Bundes. Daten stammen aus Fallzahlen der Krankenhaus-Diagnosestatistik für Deutschland, nach Alter, Mittelwerte der Jahre 2010-2013.
Invasive Pneumokokken-Erkrankungen (IPD)
Für IPD gab es lange nur eine Meldepflicht auf Landesebene (Sachsen-Anhalt, Sachsen, Mecklenburg-Vorpommern, Brandenburg und Thüringen), doch ist nun gemeinsam mit der Einführung des Masernschutzgesetzes im März 2020, eine bundesweite Meldepflicht eingeführt worden .1,16 Daher ist davon auszugehen, dass sich hier die Datenlage innerhalb der nächsten Jahre deutlich verbessern wird. Aktuell hat jedoch das RKI, wie bei CAP, nach einer individualisierten Abfrage der GBE anhand diagnostizierter IPD eine Schätzung über Auftreten (20-60Lj.: 1,7/100.000; >60Lj.: 7,6/100.000; >65Lj.: 6,4/100.000) und Sterblichkeit (20-60Lj.: 0,2/100.000; >60Lj.: 1,3/100.000; >65Lj.: 1,5/100.000) in Deutschland aufgestellt.
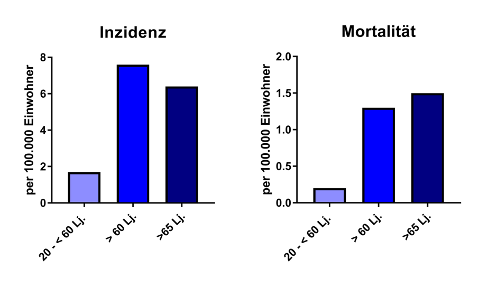
Abbildung 2: Geschätzte Inzidenz und Mortalität der invasiven Pneumokokken Erkrankungen (IPD) nach individualisierter Abfrage des RKI bei der Gesundheitsstatistik des Bundes. Daten stammen aus Fallzahlen der Krankenhaus-Diagnosestatistik für Deutschland, nach Alter, Mittelwerte der Jahre 2010 – 2013.
Darüber hinaus führt seit Januar 2007 das RKI ein webbasiertes, freiwilliges Überwachungssystem zur Überwachung von IPD.17 Die Daten der RKI deuten auf erhöhte Meldeinzidenzen bei Kindern <2 Jahren und Erwachsenen im höheren Lebensalter hin.
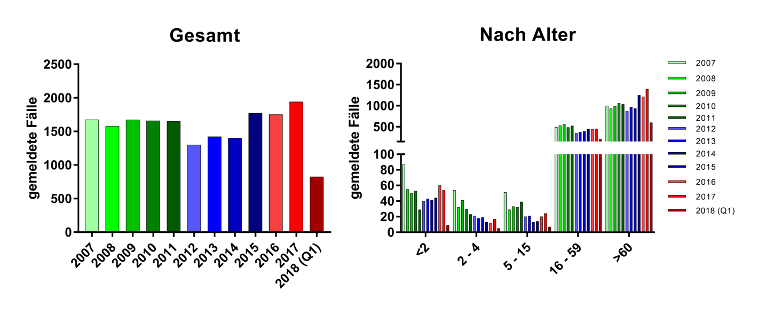
Abbildung 3: Gemeldete Fälle von Invasiven-Pneumokokken Erkrankungen ans RKI. (PneumoWeb)
Dieselben Beobachtungen konnten bereits in Ländern getroffen werden, in denen bisher bessere Überwachungssysteme bestanden.18,19
1.3 Pathogenese
Die Pathogenese des Erregers wird hier einerseits durch seine Verbreitungsmechanismen im menschlichen Körper beschrieben, andererseits durch den Schaden, den er entsprechend im lokalen Gewebe und im System auslösen kann.
Verbreitung
Angefangen durch die Tröpfcheninfektionen siedeln sich Pneumokokken zunächst im Nasenrachenraum an, wo sie normalerweise keine Symptome verursachen. Wandern die Erreger jedoch in benachbarte Strukturen, wie die Nasennebenhöhlen oder das Mittelohr, können sie dort entsprechende Entzündungsreaktionen auslösen. Der Befall des unteren Atemweges erfolgt durch Sog bei der Einatmung. Sind die Lungenbläschen erst einmal erreicht, kann die ausgelöste Entzündung Nachbarstrukturen, wie Lungenfell und Herzbeutel, befallen und in das Gefäßsystem übergehen. In den Gefäßen erreichen die Erreger die Blut-Hirn-Schranke, das Bauchfell sowie die Gelenke.20
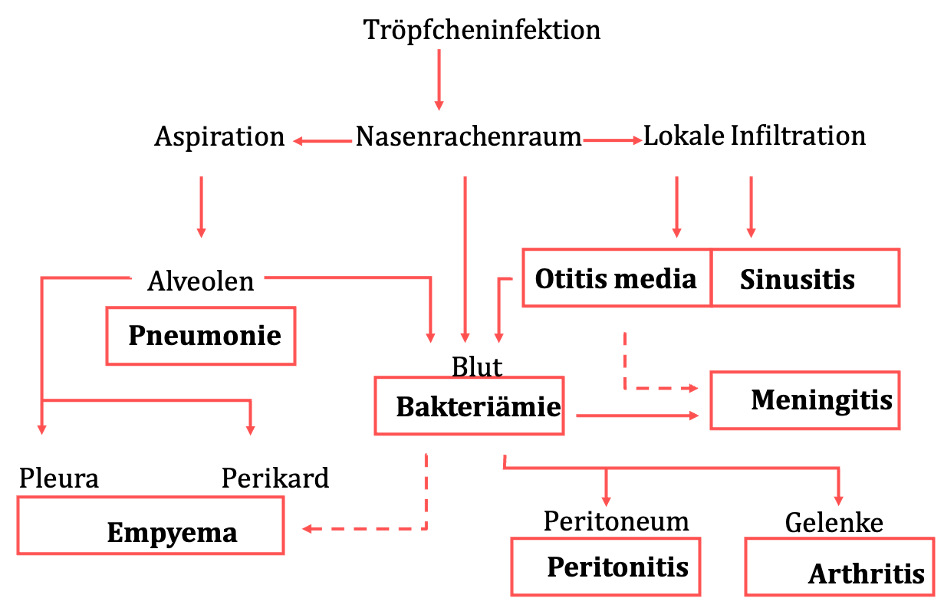
Abbildung 4: Verbreitung des Erregers
Zum Überwinden der menschlichen Abwehrmechanismen, die mit den befallenen Bereichen des Erregers einhergehen, bilden und scheiden Pneumokokken ein breites Spektrum an Schutzmolekülen aus. In den oberen und unteren Atemwegen ist die Kohlenhydratkapsel ein entscheidender Schutz vor dem Abbau durch Immunzellen. Gleichzeitig arbeiten gebildete Neuraminidasen, (Oberflächeneiweiße) daran, die Dickflüssigkeit des Schleims zu reduzieren, um die Barrierefunktion zu behindern und das Anhaften des Erregers zu stärken.4 Um den anti-bakteriellen Eiweißen des respiratorischen Epithels zu entgehen, scheiden Pneumokokken, durch das Eiweiß Autolysin LytA, ihre eigene Kapsel ab.21 Sind die Lungenbläschen erst einmal erreicht, geht man davon aus, dass eine Kombination aus Entzündung bzw. Schaden an Epithel (die oberste Zellschicht in Haut- und Schleimhautgewebe) und Endothel (innere Zellschicht der Blut- und Lymphgefäße), den Lymphwegen und die direkte Invasion des Endothels, für den Übergang ins Gefäßsystem verantwortlich sind.4 Im Blut spielt wieder die Kapsel eine enorm wichtige Rolle beim Überleben des Erregers.22 Dies erklärt auch, warum sich trotz der enorm hohen Variation der Kapselantigene, nur eine Handvoll an Serotypen im Zuge der IPD nachweisen lassen.23
Schaden
Pneumokokken bewirken im befallenen Gewebe durch die Ausscheidung entzündlicher Botenstoffe Entzündungsreaktionen und Zelluntergänge.
Pneumokokken schädigen zum einen indirekt durch entzündliche Botenstoffe wie Pneumolysin, Peptidoglykanen, Teichonsäure, Wasserstoffperoxid (H2O2) und Weitere, sowie durch die darauf folgende Aktivierung von Toll-like Rezeptor Signalwegen, Chemokin-/Zytokin-Kaskaden, dem Komplementsystem und der Gerinnungskaskade.4Zuzüglich zu der indirekten Zellschädigung durch die Entzündung, haben die Pneumokokken auch die Fähigkeit auf Wirtszellen direkt zu wirken. Zwei wichtige Vertreter sind dabei die Aminosäure Pneumolysin und das metabolische Produkt Wasserstoffperoxid.24,25 Pneumolysin ist ein Poren formendes Gift, das Nekrose verursacht.24 Seine Aktivität zeigte bisher, dass es die Reinigung der Atemwege verlangsamt, Zellkontakte unterbricht, die angeborene Immunantwort hemmt sowie für Schäden des Mittelohrs und des Gehirns verantwortlich ist.26–31 Wasserstoffperoxid ist zwar nicht so prominent wie Pneumolysin, jedoch konnte es schon in Verbindung mit Schäden der Atemwege, des Gehirns und des Herzens gebracht werden.31–34
1.4 Immunreaktion
Pneumokokken leben auf der Schleimhaut des Nasenrachenraums des Menschen und verursachen normalerweise keine Symptome, da sie vom Immunsystem gut in Schach gehalten werden können35. Die Besiedlung des Nasenrachenraums mit Pneumokokken erfolgt sehr früh, etwa bis zum 6. Lebensmonat. Nach Schätzung der ECDC (European Center of Disease Prevention and Control) sind etwa 20-40% der Kinder und 5-10% der Erwachsenen symptomlose Träger von Pneumokokken35. Breiten sich die Bakterien vom Nasenrachenraum aus, können sie Krankheiten der oberen und unteren Atemwege verursachen, wie Nasennebenhöhlen-, Mittelohr- und Lungenentzündungen35. Pneumokokken sind die häufigste Ursache von ambulant erworbenen Lungenentzündungen 36 und die häufigste Ursache von bakteriellen Lungenentzündungen bei Kindern37.
Bei Kindern unter 5 Jahren, welche Husten und/ oder Atembeschwerden mit oder ohne Fieber haben, erhärtet sich die Verdachtsdiagnose einer Lungenentzündung entweder durch schnelle Atembewegungen oder Einziehungen des Brustkorbes bei der Einatmung37. Sehr schwer erkrankte Säuglinge lassen sich möglicherweise nicht füttern bzw. stillen und können auch unter Bewusstlosigkeit, Unterkühlung und Krampfanfällen leiden37. Während die meisten Kinder eine Infektion mit ihrer natürlichen Abwehr bekämpfen können, besteht bei Kindern mit einem abgeschwächten Immunsystem ein höheres Risiko eine Lungenentzündung zu entwickeln37. Dem Erkrankungsbeginn geht häufig eine virale Infektion der Atemwege voraus (siehe unten), welche sich typischerweise mit plötzlichem hohem Fieber, Erkältung, gefolgt von Husten mit Auswurf und atemabhängigen Schmerzen präsentiert36. Säuglinge zeigen neben Husten oftmals untypische Symptome wie Trinkschwäche oder Schnupfen. Kleinkinder leiden unter Husten, schnellem Puls, sind blass und haben Fieber35. Die klinische Symptomatik ist sowohl bei Säuglingen und Kindern als auch bei Älteren und immungeschwächten Patienten weniger spezifisch36.
Bei der invasiven Pneumokokken Erkrankung (IPD) hat das Pathogen die Abwehrbarriere des Körpers durchdrungen und ist in sterile Kompartimente gelangt36. Dabei ist die Blutstrominfektion die häufigste Manifestation einer IPD, sie entsteht meist in Folge einer Pneumokokken-Lungenentzündung36. Eine Blutstromentzündung kann dabei ohne lokalisierte Symptome und spezifische Symptome auftreten, wobei insbesondere bei Erwachsenen häufig ein Infektionsherd vorliegt, von dem aus sich die Infektion weiter ausbreitet36. So kann eine Besiedlung des Blutes mit Pneumokokken-Erregern zur Auslösung einer Infektion der Hirnhäute, des Bauchfells, der Knochen, der Gelenke oder der Lunge führen36.
Die Ursache für invasive Infektionen sind dabei fast ausschließlich eingekapselte Pneumokokken-Stämme. Die Kohlenhydratkapsel ist somit ein wichtiger Faktor, der für die Schädlichkeit des Erregers verantwortlich ist und den Organismus vor dem Abbau durch Immunzellen schützt36. Das Risiko für eine schwere invasive Pneumokokken-Erkrankung ist altersabhängig. Kinder in den ersten beiden Lebensjahren und ältere Menschen sind besonders gefährdet35.
Des weiteren sind Pneumokokken die häufigste Ursache für bakterielle Hirnhautentzündungen bei Erwachsenen36. Die Invasion der Hirnhaut mit den Erregern erfolgt normalerweise über den Blutkreislauf (siehe IPD), kann jedoch auch durch direkten Eintritt nach einem Schädelbruch erfolgen36. Bei dieser gefürchteten und höchst gefährlichen Form der Pneumokokken-Erkrankung kann es neben hohem Fieber zu Kopfschmerzen, Übelkeit, Erbrechen, Lichtscheue bis hin zu Bewusstseinsstörungen, Desorientiertheit und Krämpfen kommen38. Die Patienten zeigen häufig eine schmerzhafte Nackensteifigkeit und können weiterhin fokale neurologische Defizite und Hirnnervenlähmungen aufweisen36. Die Symptome können dabei plötzlich akut oder langsam schleichend auftreten36. Im Säuglingsalter haben die Kinder hohes Fieber, Erbrechen, sind apathisch oder unruhig, verweigern die Nahrung oder erleiden Krampfanfälle. Sind die Kinder älter als ein Jahr, tritt die typische Nackensteifheit auf, darüber hinaus Kopfschmerzen und Bewusstseinsstörungen35. Kinder zeigen jedoch oft wenig charakteristische Krankheitszeichen, so dass die Beteiligung des Gehirns mitunter schwer zu erkennen sein kann38.
1.5 Therapie
In Deutschland sind Pneumokokken meist noch gut penicillinempfindlich39, weshalb das Antibiotikum der ersten Wahl bei Pneumokokken-Infektionen Penicillin ist40. Nach Beginn einer solch wirksamen antimikrobiellen Behandlung, wird angenommen, dass die Patienten weniger als 24 Stunden ansteckend bleiben36. Die Therapiedauer beträgt bei Pneumokokken-Infektionen in der Regel 5-10 Tage (bzw. weitere 3-5 Tage nach Entfieberung)41.
Aus anderen Ländern (z.B. Spanien) wird jedoch über eine Zunahme Penicillin-resistenter Pneumokokken-Infektionen berichtet39. Antibiotikaresistenzen sind europaweit ein zunehmendes Problem und in vielen Ländern kann somit nicht mehr von einer Anfälligkeit für antimikrobielle Makrolide, Penicilline und Cephalosporine ausgegangen werden36. Bei diesen Resistenzen kommt Vancomycin und evtl. Rifampicin in Betracht39, da die Pneumokokken gegen Vancomycin noch keine Resistenz entwickelt haben36.
1.6 Spätfolgen einer Infektion
Pneumokokken-Infektionen und invasive Pneumokokken Erkrankungen sind die Hauptursache für die Krankheitshäufigkeit und Sterblichkeit übertragbarer Krankheiten in Europa und weltweit, wobei die höchste Krankheitslast bei kleinen Kindern und älteren Menschen auftritt36.
Ein großer Teil der IPDs ist jedoch durch Impfstoffe vermeidbar36. Die Prognose hängt davon ab, welches Organ betroffen ist. Die Lungenentzündung hat heute eine relativ gute Prognose39. Die häufigste Komplikation einer Pneumokokken-Lungenentzündung ist eine Flüssigkeitsansammlung zwischen Lunge und Brustkorb. Lungenabszesse und Herzbeutelentzündungen infolge von lokaler Ausdehnung der Infektion sind relativ seltene, aber allgemein anerkannte Komplikationen einer Pneumokokken-Lungenentzündung36.
Trotz der guten Prognose wird die Krankenhaussterblichkeit einer Pneumokokken-Pneumonie auf 15 % geschätzt. Prognostische Faktoren sind dabei Alter, Grunderkrankungen, Ausmaß und Komplikationen der Infektion, sowie die Aktualität einer wirksamen Antibiotikatherapie36. Weltweit sterben pro Jahr etwa 1 Million Kinder an den Folgen einer Pneumokokken-Lungenentzündung38.
Die Pneumokokken-Hirnhautentzündung hat eine schlechtere Prognose als z.B. Hirnhautentzündungen durch H. influenzae oder Meningokokken39. Sie ist also mit einem höheren Risiko für Tod und dauerhafte Behinderung verbunden, als andere bakterielle Hirnhautentzündungen – ihre Sterblichkeitsrate liegt bei 10-30%36. Die Langzeitschäden nach einer Hirnhautentzündung können Taubheit, Gehirnschäden oder Lähmungen sein38. In Deutschland sterben jährlich schätzungsweise über 5000 Menschen an einer Pneumokokken-Erkrankung35.
2. Der Impfstoff
Es gibt aktuell 3 verschiedene Pneumokokken-Impfstoffe, die alle aktive Totimpfstoffe sind, da sie aus Teilen der Pneumokokkenhülle bestehen, welche die Krankheit nicht auslösen können. Sie werden alle in den Muskel gespritzt. Die Kosten werden für die von der Ständigen Impfkommission empfohlenen Personengruppen von der gesetzlichen Krankenversicherung übernommen.
Aktuell auf dem Markt sind folgende Impfstoffe:
- Pneumovax, PPSV23, Pneumokokkenpolysaccharid-Impfstoff, Kosten 33,20€ pro Einzeldosis, zugelassen seit September 2001
- Synflorix, PCV10, Pneumokokkenpolysaccharid-Konjugatimpfstoff, adsorbiert, Kosten pro Einzeldosis 52,60€, zugelassen seit April 2009
- Prevenar 13, PCV13, Pneumokokkenpolysaccharid-Konjugatimpfstoff, 13valent, adsorbiert, Kosten 76,00€ pro Einzeldosis, zugelassen seit Dezember 2009
2.1 Wirkmechanismus
Die Pneumokokken-Impfungen regen das Immunsystem zur Bildung körpereigener Antikörper an, die sich gegen die in den jeweiligen Impfstoffen enthaltenen Vielfachzucker-Antigene (Polysaccharide) der verschiedenen Kapseltypen richten und sind somit aktive Totimpfstoffe. Diese Kapselbestandteile sind im Impfstoff entweder in reiner Form oder in chemisch an ein Trägerprotein gebundener Form („konjugiert“) enthalten, die sie für das Immunsystem besser erkennbar machen. Entsprechend unterscheidet man zwischen reinen „Polysaccharidimpfstoffen“ und „Konjugatimpfstoffen“. Ein weiterer Unterschied besteht in der Anzahl der Pneumokokken-Serotypen, die im Impfstoff enthalten sind und gegen die die Impfung somit schützen soll.
Pneumokokken-Polysaccharidimpfstoffe (PPSV) gibt es bereits seit den 1970er Jahren. Der aktuell verfügbare Impfstoff enthält Antigene von 23 Serotypen und deckt somit etwa 82% der hierzulande relevanten Serotypen bei Erwachsenen ab, gegen die dieser Impfstoff immunisieren soll (PPSV23, Pneumovax®, zugelassen ab dem Alter von 2 Jahren).
Pneumokokken-Konjugatimpfstoffe (PCV) wurden später entwickelt, nachdem sich gezeigt hatte, dass die PPSV bei Kindern unter 2 Jahren, einer besonders gefährdeten Altersgruppe, keine ausreichende Immunantwort auslösen. Aktuell sind in Deutschland ein Konjugatimpfstoff gegen 10 Serotypen (PCV10, Synflorix®, zugelassen bis zum Alter von 5 Jahren) und ein Konjugatimpfstoff gegen 13 Serotypen (PCV13, Prevenar 13®, zugelassen für alle Altersgruppen, deckt ca. 63% der relevanten Serotypen ab) erhältlich.42
2.2 Inhaltsstoffe und Herstellung
Pneumovax:
- Wirkstoffe für 1 Dosis (0,5ml): je 25 Mikrogramm der 23 Typen von Polysacchariden (Mehrfachzuckern) von Pneumokokken (Typ 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 20, 22F, 23F, 33F), Phenol, Natriumchlorid, Wasser43
Synflorix:
- Wirkstoffe für eine Dosis (0,5ml): je 1 Mikrogramm Pneumokokkenpolysaccharid der Serotypen 1, 5, 6B, 7F, 9V, 14, 23F und je 3 Mikrogramm der Serotypen 4, 18C und 19F; alle Polysaccharide sind an Aluminiumphosphat adsorbiert (gesamt 0,5 Milligramm), die Polysaccharide der Serotypen 1, 4, 5, 6B, 7F, 9V und 23F sind an Protein D-Trägerprotein konjugiert, das von nicht-typisierbarem Haemophilus influenzae stammt (9-16 Mikrogramm), das Pneumokokkenpolysaccharid des Serotyp 18C ist an Tetanustoxoid-Trägerprotein konjugiert (5-10 Mikrogramm), das Polysaccharid des Serotyp 19F ist an Diphtherietoxoid-Trägerprotein konjugiert; ansonsten enthalten 1-Dosen- und 2-Dosenbehältnisse Natriumchlorid und Wasser für Injektionszwecke und das 4-Dosenbehältnis zusätzlich noch 2-Phenoxyethanol44
· Zulassungserteilung: 30.03.2009, letzte Verlängerung 22.11.2018
Prevenar 13:
Die Wirkstoffe sind Polysaccharid-CRM197-Konjugate, bestehend aus:
- 2,2 µg Polysaccharid der Serotypen 1, 3, 4, 5, 6A, 7F, 9V, 14, 18C, 19A, 19F und 23F
- 4,4 µg Polysaccharid des Serotyps 6B
- 1 Dosis (0,5 ml) enthält etwa 32 µg CRM197-Trägerprotein, adsorbiert an Aluminiumphosphat (0,125 mg Aluminium).
Die sonstigen Bestandteile sind Natriumchlorid, Bernsteinsäure, Polysorbat 80 und Wasser für Injektionszwecke.45
2.3 Impfwirkungen und -nebenwirkungen
Generell können bei Impfungen allergische Reaktionen mit beispielsweise Atembeschwerden, einem niedrigen Blutdruck, Schwindel, Fieber, Unwohlsein, Schwellungen im Gesichts- und Halsbereich, Ausschlag bis zum Kreislaufkollaps auftreten. In diesem Fall sollte man sofort einen Arzt aufsuchen.
Relativ häufig treten auch örtlich begrenzte Impfreaktionen an der Einstichstelle wie Schwellungen, Schmerzen, Rötungen, Wärmegefühl bis zu Verhärtungen auf. Weiterhin können die Lymphknoten in der Umgebung der Einstichstelle sowie die Extremität selbst anschwellen und die Bewegung einschränken. Den ganzen Körper betreffend können Fieber (teilweise mit Fieberkrämpfen), Unwohlsein, Müdigkeit, Schüttelfrost, Übelkeit, Erbrechen, Appetitlosigkeit, Reizbarkeit, Kopf- sowie Muskel- und Gelenkschmerzen auftreten.
Seltener kommt es zu einem Abfall der Blutplättchen bei Personen mit der Krankheit ITP, bei denen die Anzahl bereits von vornherein vermindert ist. Ebenso selten kommt es zu Missempfindungen der Haut, Kribbeln, Taubheitsgefühl, Schwäche in Beinen und Armen, einem Guillain-Barré-Syndrom (meist sich vollständig zurückbildende Entzündung der Nerven und Nervenwurzeln), einer Erhöhung eines Entzündungswertes im Blut (CRP), Blutarmut durch Auflösung der roten Blutkörperchen bei Patienten, die bereits früher eine derartige Erkrankung hatten (hämolytische Anämie) oder einem Anstieg bestimmter Typen von weißen Blutkörperchen.
Bei Kindern kann es nach der Impfung zu ungewöhnlichem Schreien und selten zu Atempausen bei sehr unreifen Frühgeborenen oder hypoton-hyporesponsiven Episoden (plötzliche Reduktion des Muskeltonus und des Bewusstseins) kommen.
Mehr lesen:
Pneumovax:
· Allergische Reaktionen (Atembeschwerden, blaue Lippen/Zunge, niedriger Blutdruck, Schwindel, Kreislaufkollaps, Fieber, allgemeines Unwohlsein, Schmerzen/Entzündungen/Schwellungen der Gelenke und Muskeln, Anschwellen von Gesicht/Lippen/Zunge/Hals-Rachen-Bereich/Hände/Füße/Knöchel, Nesselsucht, Ausschlag sofort einen Arzt aufsuchen; schwerwiegende allergische Reaktionen treten meist kurz nach der Verabreichung des Impfstoffs auf, wenn man noch in der Praxis ist)
- Bei 1 von 10 Geimpften: Schmerz, Hautrötung, Wärmegefühl, Schwellung und Verhärtungen an der Injektionsstelle und Fieber. (nach der Wiederholungsdosis häufiger als nach der ersten)
- Bei bis zu 1 von 1.000 Geimpften: Anschwellen der Gliedmaße, in die Impfstoff verabreicht wurde
- Häufigkeit nicht bekannt: schmerzhafte Bewegungseinschränkung der Gliedmaße, in die der Impfstoff verabreicht wurde, Müdigkeit, allgemeines Unwohlsein, Schüttelfrost, Übelkeit, Erbrechen, vergrößerte/entzündete Lymphknoten, Schmerzen/Entzündungen/Schwellungen der Gelenke, Muskelschmerzen, Abfall der Blutplättchen bei Personen mit der Krankheit ITP, bei denen Die Anzahl bereits von vornherein vermindert ist, Kopfschmerzen, Missempfindungen der Haut, Kribbeln, Taubheitsgefühl, Schwäche in Beinen und Armen, Guillain-Barré-Syndrom (meist sich vollständig zurückbildende Entzündung der Nerven und Nervenwurzeln), Erhöhung eines Entzündungswertes im Blut (CRP), Blutarmut durch Auflösung der roten Blutkörperchen bei Patienten, die bereits früher eine derartige Erkrankung hatten (hämolytische Anämie), Anstieg bestimmter Typen von weißen Blutkörperchen, Fieberkrämpfe43
Synflorix:
· Bei 1 von 10 Geimpften: Appetitlosigkeit, Reizbarkeit, Schläfrigkeit, Fieber >38°C, Schmerzen/Rötung/Schwellung an der Injektionsstelle
· Bei 1 von 100 Geimpften: Fieber > 39°C, Verhärtung an der Injektionsstelle
· Bei 1 von 1.000 Geimpften: ungewöhnliches Schreien, Atempausen bei sehr unreifen Frühgeborenen (geboren vor der vollendeten 28. SSW), Durchfall, Erbrechen, Hautausschlag, Bluterguss/Blutung/Knötchen an der Injektionsstelle, Kopfschmerzen, Übelkeit, Fieber >40°C, Schwellung der Extremität, an der die Injektion vorgenommen wurde, Juckreiz
· Bei 1 von 10.000 Geimpften: allergische Reaktionen (wie juckende Hautentzündung, Neurodermitis), Krampfanfälle (einschließlich Fieberkrämpfe), Nesselsucht, hypoton-hyporesponsive Episode (plötzliche Reduktion des Muskeltonus und des Bewusstseins)
· Selter als 1 von 10.000 Geimpften: Angioödem (sich rasch entwickelnde Schwellung der Unterhaut), Kawasaki-Syndrom (fieberhafte systemische Erkrankung durch Entzündung der kleinen und mittelgroßen Arterien), Anaphylaxie (stärkste allergische Reaktion)44
Prevenar 13:
Bei mehr als 1 von 10 Geimpften: verminderter Appetit, Fieber, Reizbarkeit, Schmerz, Berührungsempfindlichkeit, Rötung/Schwellung/Verhärtung der Einstichstelle, Schläfrigkeit, unruhiger Schlaf, Kälteschauer, Verschlechterung oder erstmaliges Auftreten von Gelenk-/Muskelschmerzen (bei Erwachsenen)
- Bei 1 von 10 Geimpften: Erbrechen, Durchfall, Fieber > 39°C, Berührungsempfindlichkeit der Einstichstelle, die die Bewegung stört, Rötung/Schwellung/Verhärtung an Einstichstelle von 2,5 - 7cm Durchmesser, Ausschlag, Kopfschmerzen, Nesselsucht (bei Jugendlichen)
- Bei 1 von 100 Geimpften: Fieberkrämpfe (Krampfanfälle), Nesselsucht (bei Säuglingen und Kleinkindern), Rötung/Schwellung/Verhärtung > 7cm Durchmesser, Weinen (Säuglinge/Kleinkinder), Übelkeit, vergrößerte Lymphknoten nahe der Einstichstelle
- Bei 1 von 1.000 Geimpften: Kollaps oder schockähnlicher Zustand (hypoton-hyporesponsive Episode), Überempfindlichkeitsreaktionen einschließlich Schwellung der Lippen und/oder des Gesichts und Atemschwierigkeiten
Mehr lesen:
Die folgenden Nebenwirkungen wurden bei Anwendung von Prevenar 13 bei Säuglingen und Kindern (im Alter von 6 Wochen bis 5 Jahren) berichtet:
Die häufigsten Nebenwirkungen (diese können bei mehr als 1 von 10 Impfungen auftreten) sind:
- verminderter Appetit
- Fieber; Reizbarkeit; Schmerz, Berührungsempfindlichkeit, Rötung, Schwellung oder Verhärtung an der Einstichstelle; Schläfrigkeit; unruhiger Schlaf
- Rötung, Verhärtung, Schwellung an der Einstichstelle von 2,5 bis 7,0 cm Durchmesser (nach der Auffrischdosis und bei älteren [2 bis 5 Jahre alten] Kindern)
Häufige Nebenwirkungen (diese können bei bis zu 1 von 10 Impfungen auftreten) sind:
- Erbrechen; Durchfall
- Fieber über 39 °C; Berührungsempfindlichkeit an der Einstichstelle, die die Bewegung stört; Rötung, Verhärtung, Schwellung an der Einstichstelle von 2,5 bis 7 cm Durchmesser (nach der Grundimmunisierung)
- Ausschlag
Gelegentliche Nebenwirkungen (diese können bei bis zu 1 von 100 Impfungen auftreten) sind:
- Krämpfe (oder Krampfanfälle), einschließlich solcher, die durch hohes Fieber verursacht werden
- Nesselsucht (Urtikaria oder Urtikaria-ähnlicher Ausschlag)
- Rötung, Schwellung oder Verhärtung an der Einstichstelle von mehr als 7 cm Durchmesser; Weinen
Seltene Nebenwirkungen (diese können bei bis zu 1 von 1.000 Impfungen auftreten) sind:
- Kollaps oder schockähnlicher Zustand (hypoton-hyporesponsive Episode)
- Überempfindlichkeitsreaktionen (allergische Reaktionen), einschließlich Schwellung des Gesichts und/ oder der Lippen, Schwierigkeiten beim Atmen
Die folgenden Nebenwirkungen wurden bei Anwendung von Prevenar 13 bei Kindern und Jugendlichen (im Alter von 6 bis 17 Jahren) berichtet:
Die häufigsten Nebenwirkungen (diese können bei mehr als 1 von 10 Impfungen auftreten) sind:
- verminderter Appetit
- Reizbarkeit; Schmerz, Berührungsempfindlichkeit, Rötung, Schwellung oder Verhärtung an der Einstichstelle; Schläfrigkeit; unruhiger Schlaf; Berührungsempfindlichkeit an der Einstichstelle, die die Bewegung stört
Häufige Nebenwirkungen (diese können bei bis zu 1 von 10 Impfungen auftreten) sind:
- Kopfschmerzen
- Erbrechen; Durchfall
- Ausschlag; Nesselsucht (Urtikaria oder Urtikaria-ähnlicher Ausschlag)
- Fieber
Kinder und Jugendliche mit HIV-Infektion, Sichelzellkrankheit oder Blutstammzelltransplantation hatten ähnliche Nebenwirkungen, jedoch traten Kopfschmerzen, Erbrechen, Durchfall, Fieber, Müdigkeit, Gelenk- und Muskelschmerzen sehr häufig auf.
Die folgenden weiteren Nebenwirkungen wurden nach der Markteinführung von Prevenar 13 bei Säuglingen und Kindern im Alter von bis zu 5 Jahren beobachtet:
- schwere allergische Reaktionen, einschließlich Schock (Herz-Kreislauf-Kollaps); Angioödem (Schwellung der Lippen, des Gesichtes oder des Rachens)
- Nesselsucht (Urtikaria), Hautrötung und -reizung (Dermatitis) und Juckreiz (Pruritus) an der Einstichstelle; Hautrötung (im Gesicht und/ oder am Körper)
- vergrößerte Lymphknoten oder -drüsen (Lymphadenopathie) in der Nähe der Einstichstelle, z. B. unter dem Arm oder in der Leistenbeuge
- Ausschlag, bei dem juckende rote Flecken entstehen (Erythema multiforme)
Bei sehr unreifen Frühgeborenen (Geburt in oder vor der 28. Schwangerschaftswoche) können innerhalb von 2 bis 3 Tagen nach der Impfung längere Atempausen auftreten.
Die folgenden Nebenwirkungen wurden unter Prevenar 13 bei Erwachsenen berichtet:
Die häufigsten Nebenwirkungen (diese können bei mehr als 1 von 10 Impfungen auftreten) sind:
- verminderter Appetit; Kopfschmerzen; Durchfall; Erbrechen (bei Erwachsenen zwischen 18 und 49 Jahren)
- Kälteschauer; Müdigkeit; Ausschlag; Schmerzen, Rötung, Schwellung, Verhärtung oder Berührungsempfindlichkeit an der Einstichstelle, die die Armbewegung stört (starke Schmerzen oder Berührungsempfindlichkeit an der Einstichstelle bei Erwachsenen zwischen 18 und 39 Jahren und starke Beeinträchtigungen der Beweglichkeit des Arms bei Erwachsenen zwischen 18 und 39 Jahren)
- Verschlechterung oder erstmaliges Auftreten von Schmerzen in Ihren Gelenken oder Muskeln
- Fieber (bei Erwachsenen zwischen 18 und 29 Jahren)
Häufige Nebenwirkungen (diese können bei bis zu 1 von 10 Impfungen auftreten) sind:
- Erbrechen (bei Erwachsenen im Alter von 50 Jahren und darüber); Fieber (bei Erwachsenen im Alter von 30 Jahren und darüber)
Gelegentliche Nebenwirkungen (diese können bei bis zu 1 von 100 Impfungen auftreten) sind:
- Übelkeit
- Überempfindlichkeitsreaktionen (allergische Reaktionen), einschließlich Schwellung des Gesichts und/ oder der Lippen, Schwierigkeiten beim Atmen
- vergrößerte Lymphknoten oder drüsen (Lymphadenopathie) nahe der Einstichstelle, wie z. B. unter dem Arm
Erwachsene mit HIV-Infektion hatten ähnliche Nebenwirkungen, jedoch traten Fieber und Erbrechen sehr häufig auf, und Übelkeit trat häufig auf.
Erwachsene mit Blutstammzelltransplantation hatten ähnliche Nebenwirkungen, jedoch traten Fieber und Erbrechen sehr häufig auf.45
3. Aktuelles
Während der SARS-CoV-2-Pandemie wird die Pneumokokken-Impfung für Ältere und chronisch kranke Menschen von Ärzten und Behörden verstärkt über öffentliche Medien empfohlen. So soll verhindert werden, dass sich Patienten mit zwei Erkrankungen gleichzeitig anstecken, die die Lunge schädigen können und Komplikationen im Krankheitsverlauf wahrscheinlicher machen würden. Neben der Pneumokokken-Impfung gilt diese Empfehlung auch für die Grippe- und Keuchhusten-Impfung. Die Nachfrage nach den Impfstoffen stieg daraufhin so enorm, dass es teilweise zu Lieferengpässen kam.46
4. Auffrischung und Impfung im späteren Lebensalter
Neben der Grundimmunisierung in den ersten 2 Lebensjahren wird eine Pneumokokken-Impfung auch für Menschen über 60 Jahre sowie Menschen mit chronischen Erkrankungen des Herzens, der Lunge, einer behandlungspflichtigen Zuckerkrankheit, bestimmten neurologischen Erkrankungen, einem unzureichenden Immunsystem, einer Hörprothese (Cochlea-Implantat) oder einer Verbindung zwischen dem Hirnnervenwassersystem und der Außenwelt (Liquorfistel) empfohlen.
Ab dem 16. Lebensjahr wird für die Impfung der 23-valente Polysaccharidimpfstoff Pneumovax 23 empfohlen. Zwischen dem 2. und 15. Lebensjahr wird angeraten, zunächst eine Impfung mit dem Konjugatimpfstoff Prevenar 13 vorzunehmen und 6 Monate später auf Pneumovax 23 umzusteigen, um einen größtmöglichen Impfschutz zu erreichen.
Chronisch kranken Patienten wird empfohlen, den Impfschutz anschließend alle 6 Jahre mit Pneumovax 23 aufzufrischen. Bei Patienten ohne eine der oben genannten Erkrankungen soll die Rechtfertigung für eine Auffrischimpfung individuell geprüft und mit den möglichen Nebenwirkungen abgewogen werden.
Sofern keine Risikoerkrankungen vorliegen, soll eine verpasste Impfung nach den ersten 2 Lebensjahren nicht nachgeholt werden, sondern erst wieder gemäß dem Impfkalender ab dem 60. Lebensjahr geimpft werden.47,48
5. STIKO-Empfehlungen
Die Ständige Impfkommission ist eine ehrenamtliche, politisch und weltanschaulich unabhängige Expertengruppe in der Bundesrepublik Deutschland, welche auf wissenschaftlicher Grundlage Empfehlungen für die notwendigen Schutzimpfungen in Deutschland ausspricht. Seit 1998 besteht die Empfehlung zur einmaligen Impfung der über 60-Jährigen mit dem Polysaccharidimpfstoff sowie zur Impfung von chronisch Kranken alle 6 Jahre. Die Empfehlung zur Standardimpfung in den ersten 2 Lebensjahren wurde 2006 von der STIKO ausgesprochen. Geimpft werden soll zu diesem Zeitpunkt mit dem Konjugatimpfstoff im 2. Lebensmonat, im 4. Lebensmonat und im 11. Lebensmonat, Frühgeborene sollen ab dem 2. Lebensmonat 3 Impfdosen im 4-Wochen Abstand erhalten sowie eine weitere Dosis im 11. Lebensmonat.
Begründet wurde die Empfehlung vor allem durch den Umstand, dass laut WHO Pneumokokken der weltweit bedeutendste bakterielle Krankheitserreger sind und weltweit für über 1 Millionen Tode von Kindern mitverantwortlich ist. Auch in einem industriellen Land wie Deutschland starben zum Zeitpunkt der ersten Impfempfehlung etwa 20 Kinder jährlich an den Folgen einer Pneumokokkeninfektion, weitere 20 hatten bleibende Schäden und zahlreiche Kinder mussten aufgrund von Komplikationen in ein Krankenhaus aufgenommen werden. Auch bei Erwachsenen wurde als Impfziel die Reduktion von schweren Pneumokokkeninfektionen mit den damit einhergehenden Risiken für Krankenhausaufenthalte, bleibende Schäden und Tod definiert. Ein weiteres sich anbahnendes Problem, das durch die Impfung gebremst werden soll, ist die zunehmende Antibiotikaresistenz der Pneumokokken.
Auch wenn die STIKO Wiederholungsimpfungen alle 6 Jahre auch für alle Menschen über 60 als sinnvoll erachtet, kann derzeit noch keine generelle Empfehlung ausgesprochen werden, da in früheren Studien ein erhöhtes Risiko für Lokalreaktionen bei häufigeren Impfungen beschrieben wurde. Dieses Risiko konnte in späteren Studien nicht bestätigt werden, allerdings wurde in der Fachinformation von Pneumovax 23 diese Einschränkung noch nicht wieder revidiert.49
6. Impfempfehlungen in anderen Ländern
Eine Empfehlung zur Impfung von allen Kindern unter 2 Jahren mit dem Polysaccharidimpfstoff besteht nahezu weltweit. Ausnahmen stellen zum Beispiel Moldawien, Estland, Indien und Teile Indonesiens dar. Uneinig sind sich die Länder, wann und wie oft geimpft werden soll: einige beginnen erst im 3. Lebensmonat, andere schon in der 6. Lebenswoche, viele impfen 3 mal, einige auch 4 mal. In einigen Ländern besteht eine Impfpflicht, darunter auch Frankreich und Ungarn.
Die Empfehlung zur Impfung von chronisch Kranken und Menschen ab dem 50.-65. Lebensjahr mit dem Polysaccharidimpfstoff besteht überwiegend in industriell weit entwickelten Ländern. 50,51
7. Quellen
(1)Robert Koch-Institut. Wissenschaftliche Begründung zur Änderung der Pneumokokken-Impfempfehlung für Säuglinge. Mitteilung der Ständigen Impfkommission (STIKO) am RKI (2015) doi:10.17886/EPIBULL-2015-005.
(2) Paton, J. C. & Trappetti, C. Streptococcus pneumoniae Capsular Polysaccharide. Microbiol Spectr 7, (2019).
(3) Varghese, R., Jayaraman, R. & Veeraraghavan, B. Current challenges in the accurate identification of Streptococcus pneumoniae and its serogroups/serotypes in the vaccine era. J. Microbiol. Methods 141, 48–54 (2017).
(4) Loughran, A. J., Orihuela, C. J. & Tuomanen, E. I. Streptococcus pneumoniae: Invasion and Inflammation. Microbiol Spectr 7, (2019).
(5) Torres, A. et al. Burden of pneumococcal community-acquired pneumonia in adults across Europe: A literature review. Respir Med 137, 6–13 (2018).
(6) Fitzgerald, D. & Waterer, G. W. Invasive Pneumococcal and Meningococcal Disease. Infect. Dis. Clin. North Am. 33, 1125–1141 (2019).
(7) Oligbu, G., Fry, N. K. & Ladhani, S. N. The Epidemiology and Biostatistics of Pneumococcus. Methods Mol. Biol.1968, 215–224 (2019).
(8) Weiser, J. N., Ferreira, D. M. & Paton, J. C. Streptococcus pneumoniae: transmission, colonization and invasion. Nat. Rev. Microbiol. 16, 355–367 (2018).
(9) Domenech de Cellès, M. et al. Unraveling the seasonal epidemiology of pneumococcus. Proc. Natl. Acad. Sci. U.S.A. 116, 1802–1807 (2019).
(1)0Disease factsheet about pneumococcal disease. European Centre for Disease Prevention and Control https://www.ecdc.europa.eu/en/pneumococcal-disease/facts.
(11)§ 6 IfSG - Einzelnorm.
(12) § 7 IfSG - Einzelnorm.
(13) van Hoek, A. J. et al. Pneumococcal carriage in children and adults two years after introduction of the thirteen valent pneumococcal conjugate vaccine in England. Vaccine 32, 4349–4355 (2014).
(14) GBD 2016 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet 390, 1211–1259 (2017).
(15) Welte, T., Torres, A. & Nathwani, D. Clinical and economic burden of community-acquired pneumonia among adults in Europe. Thorax 67, 71–79 (2012).
(16) Küpke, N., Matysiak-Klose, D., Siedler, A., Wiechmann, O. & Diercke, M. Gesetz für den Schutz vor Masern und zur Stärkung der Impfprävention (Masernschutzgesetz). (2020) doi:10.25646/6526.
(17) RKI - Pneumoweb-Sentinel. https://www.rki.de/DE/Content/Infekt/Sentinel/Pneumoweb/Pneumoweb_node.html#doc2378878bodyText2.
(18) Marrie, T. J., Tyrrell, G. J., Majumdar, S. R. & Eurich, D. T. Effect of Age on the Manifestations and Outcomes of Invasive Pneumococcal Disease in Adults. Am. J. Med. 131, 100.e1-100.e7 (2018).
(19) Rose, M. A., Christopoulou, D., Myint, T. T. H. & Schutter, I. de. The burden of invasive pneumococcal disease in children with underlying risk factors in North America and Europe. International Journal of Clinical Practice 68, 8–19 (2014).
(20) Bogaert, D., de Groot, R. & Hermans, P. Streptococcus pneumoniae colonisation: the key to pneumococcal disease. The Lancet Infectious Diseases 4, 144–154 (2004).
(21) Kietzman, C. C., Gao, G., Mann, B., Myers, L. & Tuomanen, E. I. Dynamic capsule restructuring by the main pneumococcal autolysin LytA in response to the epithelium. Nature Communications 7, 10859 (2016).
(22) Magee, A. D. & Yother, J. Requirement for Capsule in Colonization by Streptococcus pneumoniae. Infect Immun69, 3755–3761 (2001).
(23) Amin-Chowdhury, Z. et al. Characteristics of invasive pneumococcal disease (IPD) caused by emerging serotypes after the introduction of the 13-valent pneumococcal conjugate vaccine (PCV13) in England; prospective observational cohort study, 2014-18. Clin. Infect. Dis. (2020) doi:10.1093/cid/ciaa043.
(24) Berry, A. M. & Paton, J. C. Additive attenuation of virulence of Streptococcus pneumoniae by mutation of the genes encoding pneumolysin and other putative pneumococcal virulence proteins. Infect. Immun. 68, 133–140 (2000).
(25) Spellerberg, B. et al. Pyruvate oxidase, as a determinant of virulence in Streptococcus pneumoniae. Mol. Microbiol.19, 803–813 (1996).
(26) Effect of Streptococcus pneumoniae on human respiratory epithelium in vitro. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC313834/.
(27) Rayner, C. F. et al. Interaction of pneumolysin-sufficient and -deficient isogenic variants of Streptococcus pneumoniae with human respiratory mucosa. Infect. Immun. 63, 442–447 (1995).
(28) Paton, J. C. & Ferrante, A. Inhibition of human polymorphonuclear leukocyte respiratory burst, bactericidal activity, and migration by pneumolysin. Infect Immun 41, 1212–1216 (1983).
(29) Cockeran, R., Theron, A. J., Feldman, C., Mitchel, T. J. & Anderson, R. Pneumolysin potentiates oxidative inactivation of alpha-1-proteinase inhibitor by activated human neutrophils. Respir Med 98, 865–871 (2004).
(30) Comis, S. D. et al. Cytotoxic effects on hair cells of guinea pig cochlea produced by pneumolysin, the thiol activated toxin of Streptococcus pneumoniae. Acta Otolaryngol. 113, 152–159 (1993).
(31) Braun, J. S. et al. Pneumococcal pneumolysin and H(2)O(2) mediate brain cell apoptosis during meningitis. J. Clin. Invest. 109, 19–27 (2002).
(32) Hirst, R. A. et al. Effect of pneumolysin on rat brain ciliary function: comparison of brain slices with cultured ependymal cells. Pediatr. Res. 47, 381–384 (2000).
(33) Relative roles of pneumolysin and hydrogen peroxide from Streptococcus pneumoniae in inhibition of ependymal ciliary beat frequency - PubMed. https://pubmed.ncbi.nlm.nih.gov/10678974/.
(34) Brissac, T., Shenoy, A. T., Patterson, L. A. & Orihuela, C. J. Cell Invasion and Pyruvate Oxidase-Derived H2O2 Are Critical for Streptococcus pneumoniae-Mediated Cardiomyocyte Killing. Infect. Immun. 86, (2018).
(35) https://dgk.de/impfen-und-infektionen/krankheiten-von-a-bis-z/pneumokokken-infektion.html ; Pneumokokken-Erkrankung, Deutsches Grünes Kreuz e.V.
(36) https://www.ecdc.europa.eu/en/pneumococcal-disease/facts Disease factsheet about pneumococcal disease, European Centre for Disease Prevention and Control
(37) https://www.who.int/en/news-room/fact-sheets/detail/pneumonia; Pneumonia, World Health Organization
(38) https://www.sozialministerium.at/Themen/Gesundheit/Uebertragbare-Krankheiten/Infektionskrankheiten-A-Z/Pneumokokken.html; Pneumokokken, Bundesministerium (Austria)
(39) Gortner, Meyer (2018) Pädiatrie Duale Reihe, 5. Auflage, Seite 634
(40) https://web.archive.org/web/20101024230905/ http://www.zct-berlin.de/klinik.praxis/streptoPneumoniae.html ; Streoptococcus pneumoniae, Zeitschrift für Chemotherapie
(41) https://ladr.de/beratung/infektiologie/erreger_a-z/pneumokokken ; Infektion durch Pneumokokken, Der Laborverbund Dr. Kramer & Kollegen
(42) RKI. (23. Juni 2020). rki.de.
(43) Gebrauchsinformation. (Juli 2019). patieninfo-service.de. Gebrauchsinformationsverzeichnis Deutschland: https://www.patienteninfo-service.de/a-z-liste/pq/pneumovaxR-23-injektionsloesung-in-einer-fertigspritze/
(44) Fachinformation. (November 2018). gsk-arzneimittel.de.
(45) patienteninfo-service.de. (Juni 2019). Gebrauchsinformationsverzeichnis Deutschland: https://www.patienteninfo-service.de/a-z-liste/pq/prevenar-13-injektionssuspension/
(46) https://www.aerzteblatt.de/treffer?mode=s&wo=17&typ=16&aid=213188&s=pneumokokken
(47) https://www.rki.de/SharedDocs/FAQ/Impfen/Pneumokokken/FAQ-Liste_Pneumokokken_Impfen.html
(48) https://www.rki.de/DE/Content/Infekt/EpidBull/Archiv/2020/Ausgaben/34_20.pdf?__blob=publicationFile
(50) https://apps.who.int/immunization_monitoring/globalsummary/schedules